协和神经肿瘤周刊
第86期

原文链接:https://www.nature.com/articles/s41467-024-48416-9
【编译者按】
胶质母细胞瘤 (Glioblastoma, GBM) 是成人中最常见的恶性原发性脑肿瘤。标准护理 (SOC) 治疗包括最大可行切除、外照射放射治疗 (RT) 和替莫唑胺 (TMZ) 辅助治疗。表现出未甲基化 O 6 -甲基鸟嘌呤 DNA 甲基转移酶 (MGMT) 启动子的肿瘤本质上对化疗具有耐药性。除年龄和临床表现外,肿瘤切除范围是独立的预后因素。据估计,肿瘤完全切除的患者比不完全切除的患者存活 1 年的可能性高 61%。
肿瘤切除后残留的肿瘤细胞及其独特的放射治疗后肿瘤微环境,可以通过血管建成(vasculogenesis)有效恢复被治疗破坏的肿瘤血管系统。不同于血管新生(angiogennesis)依赖于血管内皮生长因子(VEGF)介导的已有血管局部增生,血管建成依赖骨髓祖细胞 (BMDC) 实现血管从头发生。在此过程中,BMDC的募集需要CXCR4/CXCR7配体CXCL12介导,因此CXCL12参与GBM不完全切除后复发过程。此外,CXCL12还被怀疑可以排斥或隔离T细胞,从而促进GBM细胞侵袭与凋亡。
在动物实验中,聚乙二醇化 L-RNA 适配体 olaptesed pegol (NOX-A12) 靶向 CXCL12 在高度难治性 GBM 的大鼠脑肿瘤模型中非常有效。为了评估 RT 联合 NOX-A12 的临床安全性和有效性,研究者进行了一项开放标签、多中心 I/II 期试验GLORIA 试验 (NCT04121455)。2024年5月28日发表在Nature Communications杂志的论文报告了该试验的剂量递增部分的结果以及肿瘤组织生物标志物依赖性结果的事后分析。
研究方法
患者入选标准
GLORIA 试验 (NCT04121455) 是一项多中心 I/II 期试验,旨在评估 RT 与连续静脉注射NOX-A12相结合的安全性和有效性。用NOX-A12治疗新诊断、不完全切除或活检的缺乏MGMT启动子甲基化的GBM(CNS WHO 4级)(图 1a)。
治疗方案
该试验包括此处报告的完整的 NOX-A12 剂量递增部分,以及正在进行的附加治疗方案的多个扩展组(此处未报告)。在剂量递增部分,NOX-A12 采用修改后的基于 3 + 3规则的设计进行给药,剂量水平 (DL) 递增为每周 200、400 和 600 mg NOX-A12。
2019 年 9 月至 2021 年 9 月期间,每个 DL 招募了 3 名患者。DL 3 的一名患者提前退出并被替换以确保安全数据质量,因此总共有 10 名患者接受了 RT 和 NOX-A12 治疗(图 1b)。诊断时的中位年龄为 65 岁(范围 43-79 岁)。10名患者中有8名接受了部分切除,其中2名不适合切除,仅接受了活检。7 名患者接受正常分割放疗,3 名患者接受大分割放疗。
应答评估
该试验的主要终点是安全性。
次要终点包括最大耐受剂量 (MTD)、推荐 II 期剂量 (RP2D)、NOX-A12 血浆水平、复发情况、肿瘤血管化、神经肿瘤学神经系统评估 (NANO)、生活质量 (QOL)、中位 PFS 、6 个月的 PFS 和 OS。此外,通过多重免疫荧光(mIF)成像对手术期间获得的肿瘤组织进行了探索性事后分析。
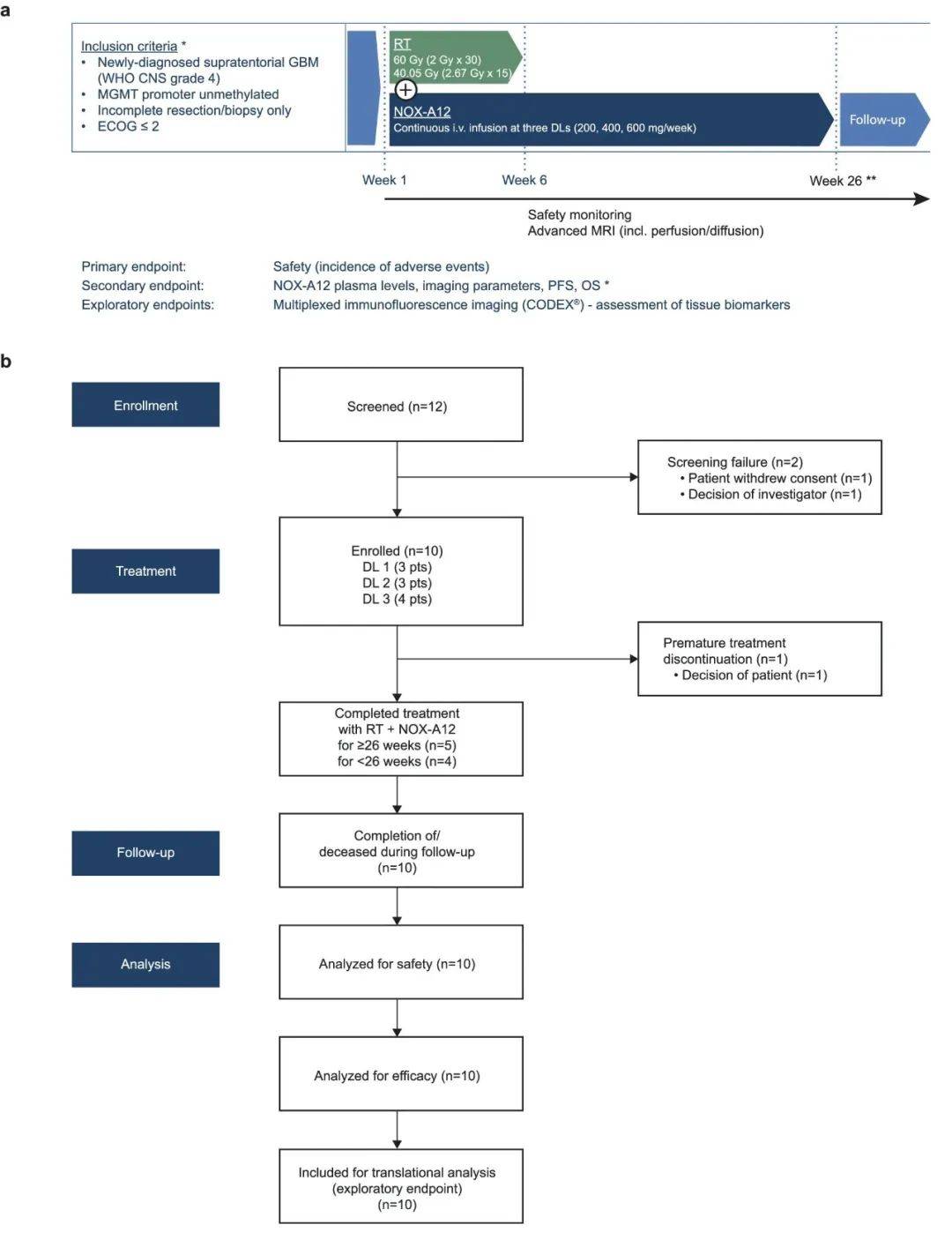
图1. GLORIA试验研究大纲
结果
药代动力学和安全性
所有患者的 NOX-A12 血浆水平在大约一周后达到稳定状态并超过 1.5 µM,这被认为是破坏 CXCL12 介导的迁移同时最大限度地减少骨髓细胞动员所需的最低血浆水平(图2a)。无患者由于严重不良反应退出试验。RT与NOX-A12联合治疗在各剂量水平中安全且耐受性良好。因此,MTD为未达到,并将600 mg每周给药作为NOX-A12的推荐II期剂量。
放射学反应
参与试验剂量递增部分的所有 10 名患者均被考虑进行反应分析。作为典型的反应性患者,C1-003 按照方案连续接受 NOX-A12 治疗 26 周,在第 9 周达到部分缓解 (PR),并在治疗结束时复发(图2b)。在 NOX-A12 下,9 名患者 (90%) 在至少一个随访时间点显示出 MRI 病灶大小的放射学反应。在基线 MRI 评估中出现目标病变 (TL) 的 9 名患者中,有 8 名 (89%) 在 NOX-A12 治疗期间显示出 TL 反应,其中 4 名 (44%) 根据放射学 mRANO 标准达到 PR。其中,两名患者分别接受 DL 1 和 DL 3 的治疗。DL 1 的所有三名患者和 DL 3 的所有四名患者的至少一个非目标病变 (NTL) 的尺寸减小了 ≥50%(图2c,d)。进一步,利用先进的MRI参数,研究者对阈值计算的高分数肿瘤负荷(FTBHigh)与表观扩散系数(ADC)进行了评估,显示NOX-A12对于肿瘤的抑制效果(图2e,f)。
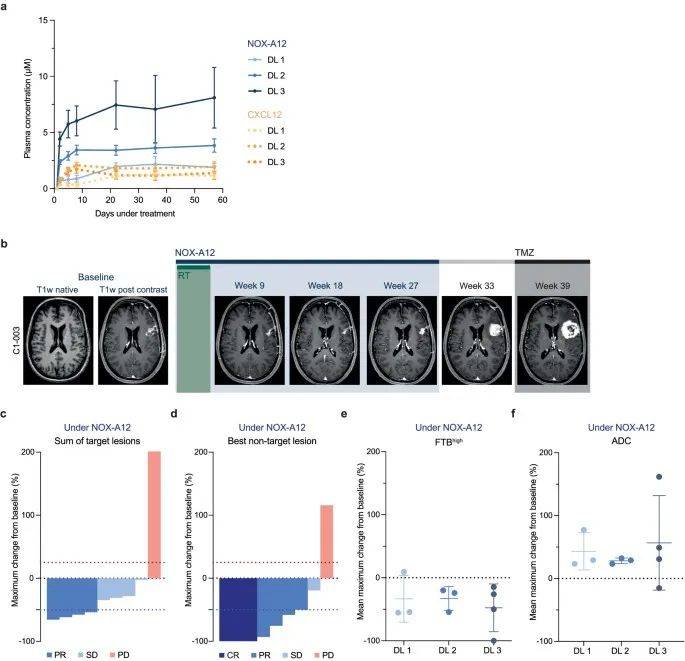
图2. RT 和 NOX-A12 治疗是安全的,并且在传统和先进 MRI 中显示放射学反应。
临床终点
整个 GLORIA 队列的中位 PFS 为 174 天(范围 58-260 天),6 个月 PFS 为 40.0%,中位 OS 为 389 天(范围144-562 天;补充图 3)。这种高变异性促使开展探索性分析,以寻找与 NOX-A12 治疗反应相关的潜在生物标志物,重点关注 CXCL12(NOX-A12 的靶标)。
生物标志物依赖性生存分析
分析来自人类 GBM的公开单细胞 RNA 测序 (scRNAseq) 数据显示,内皮细胞中 CXCL12 mRNA 表达水平和频率最高,其次是周细胞、骨髓细胞(巨噬细胞、小胶质细胞)和神经胶质瘤细胞(图3a)。因此,研究者决定在事后分析中评估从 GLORIA 患者 (n = 10) 获得的治疗前肿瘤样本中的总 CXCL12 蛋白表达和细胞类型特异性 CXCL12 蛋白表达。作为外部对照,对来自独立队列的 GBM 患者的治疗前肿瘤样本进行了相同的分析,这些患者与GLORIA患者具有相似的临床和组织学特征,接受标准(SOC) 治疗。
在后续的数据分析中,研究者利用多重免疫荧光成像技术,以细胞类型特异性方式确定 CXCL12 表达状态(图3b,c)。结果显示, GLORIA 队列中 CXCL12+细胞(总细胞)的频率与 PFS 之间存在显着正相关(rs= 0.712,p= 0.039),而SOC 队列中不存在这种相关性(图3e)。通过分析每种细胞类型的 CXCL12 阳性率,研究者发现 CXCL12+内皮细胞的频率 (E12;rs=0.695,p=0.046) 和 CXCL12+神经胶质瘤细胞(G12;rs=0.712,p=0.039)在 GLORIA 试验中入组的患者与 PFS具有显著相关性。但 CXCL12+Mφ 频率(M12;rs= 0.458,p=0.223)和 CXCL12+周细胞频率(P12;rs= 0.559,p=0.126)与PFS未达到显著相关性(图3f)。重要的是, CXCL12 + 细胞的任何特定细胞类型频率与 SOC 队列的 PFS 之间没有显着相关性(rs= 0.015,p=0.946 )
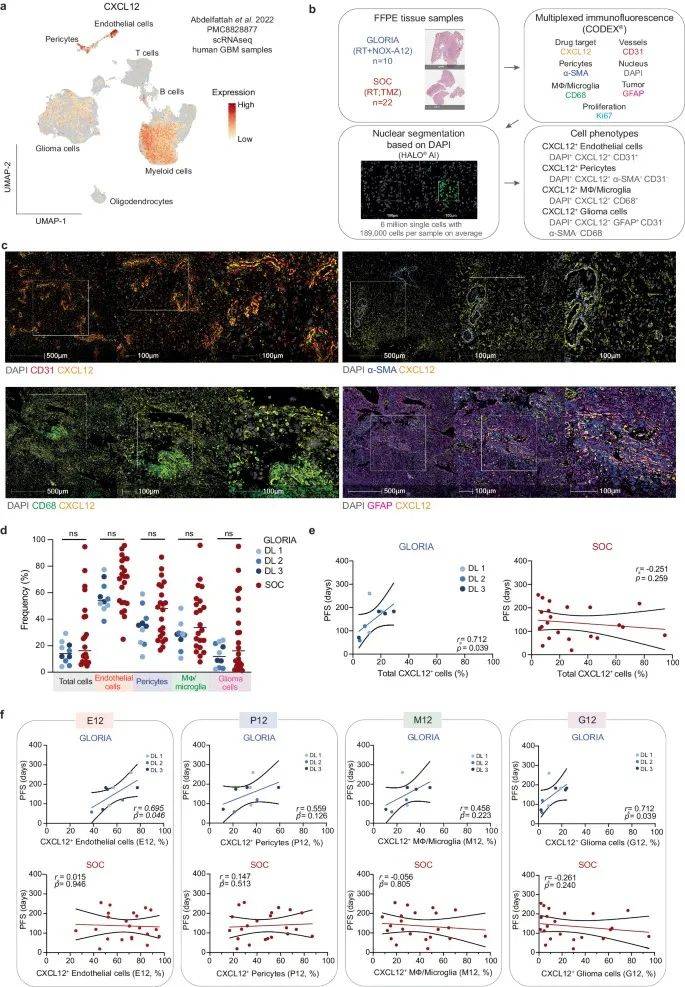
图3. GLORIA 队列中内皮细胞和神经胶质瘤细胞中的 CXCL12 阳性与 PFS 相关。
内皮细胞 (E12) 和神经胶质瘤细胞 (G12) 均与 PFS 显着相关。虽然内皮细胞表现出最高的相对 CXCL12 阳性率,但内皮细胞总数大约比神经胶质瘤细胞低12倍。研究者计算了 E12 和 G12 的中位数平均值,从而得出综合的EG12 分数。在这里,综合 EG12 评分与 GLORIA 患者的 PFS 密切相关(rs=0.865;p= 0.005;图 4a)。同样,在 SOC 队列中,研究者发现综合 EG12 评分与 PFS 之间没有显着相关性(rs=-0.133;p= 0.556;图 4b)。接下来,研究者使用 EG12 评分通过无偏中值分类器将 GLORIA 和 SOC 队列的患者分为 EG12high和 EG12low亚组。GLORIA 队列中 EG12high 患者的中位 PFS 为 183 天 vs. 92 天,其 PFS 显着长于 EG12low患者(HR 0.12(95% 置信区间 0.01–0.81);图4c)。E12 high的 OS 比 E12lowGLORIA 患者的 OS 延长的趋势(中位 OS 481 天 vs. 338 天;HR 0.25 (95% CI 0.03–1.17);p = 0.075;图 4d)。在 SOC 队列中,E12high患者和E12low患者PFS 没有显着差异(中位 PFS 118 vs. 136 天;HR 1.25(95% CI 0.51–3.12);对数秩检验,p=0.628;图 4e) 。

图4. EG12 与 PFS 相关,并且与 GLORIA 中生存率的提高相关,但与 SOC 队列中无关。
讨论
在本研究中报告了 RT 和 NOX-A12 在新诊断的化疗耐药性 GBM 中的安全性,达到了试验的主要终点。此外,事后肿瘤组织分析表明,这种抑制 CXCL12 的 L-RNA 适体在以内皮细胞和神经胶质瘤细胞 CXCL12 阳性频率高为特征的患者亚组中的临床疗效有所改善。
NOX-A12 的作用模式强烈表明,持续且不间断的治疗对于预防复发至关重要,因为只有最初的放疗才会导致肿瘤微环境的血管消失,而 NOX-A12 输注的中断可能会导致肿瘤微环境的快速重建,几周内发生 CXCL12 梯度和连续血管生成 。因此,由于治疗中断或缩减,NOX-A12 对 GBM 控制的影响可能没有得到充分利用,特别是在一些有反应的患者中。
GLORIA 试验选择的 DL 得到了安全性和有效性考虑的支持,因为 200mg/周的 NOX-A12 剂量预计会在稳态时产生药理学相关的平均血浆水平。因此,NOX-A12 治疗导致所有 DL 中药物过量超过目标血浆水平,这可能解释了该试验中缺乏剂量依赖性的原因。最高 DL 600mg NOX-A12/周是安全且耐受性良好的。
虽然 GLORIA 试验由于伦理原因仅招募了缺乏 MGMT 甲基化的患者(尚未证明 SOC 与 TMZ 的益处),但没有理由否定 NOX-A12 在 MGMT 甲基化 GBM 中的作用。因此,有必要进行确认试验,继续根据 EG12 评分来评估患者的结果。
参考文献
Giordano, F.A., Layer, J.P., Leonardelli, S., Friker, L.L., Turiello, R., Corvino, D., Zeyen, T., Schaub, C., Müller, W., Sperk, E., et al. (2024). L-RNA aptamer-based CXCL12 inhibition combined with radiotherapy in newly-diagnosed glioblastoma: dose escalation of the phase I/II GLORIA trial. Nat Commun 15, 4210. https://doi.org/10.1038/s41467-024-48416-9.
本期译者

北京协和医院神经外科、北京协和医学院临床八年制2020级钟子涵
本期编审
北京协和医院神经外科主任医师王裕副教授,医学博士、留美博士后
联系我们
北京协和医院神经外科恶性肿瘤专家出诊时间:
马文斌主任医师 周四上午特需门诊。
王裕主任医师 周二下午特需门诊。(建议想进行治疗方案咨询或参加临床试验咨询的患者选择上述门诊时间进行面诊。)
北京协和医院神经外科恶性肿瘤专家出诊时间:
马文斌主任医师 周四上午特需门诊。
王裕主任医师 周二下午特需门诊。(建议想进行治疗方案咨询或参加临床试验咨询的患者选择上述门诊时间进行面诊。)
文献编译 | 伊匹单抗与纳武单抗联合治疗脑胶质瘤I期临床试验结果公布
文献编译 | 索拉非尼、丙戊酸和西地那非治疗复发性高级别胶质瘤的2期研究 - 协和神经肿瘤周刊
文献编译| 抗PD-1治疗失败的复制修复缺陷型胶质瘤患者 接受免疫联合治疗仍可能改善预后 - 协和神经肿瘤周刊
协和神经肿瘤周刊汇总(总82期)
协和神经肿瘤周刊
《协和神经肿瘤周刊》由北京协和医院神经外科与神外前沿新媒体共同采写制作,报道本领域最新前沿进展,学术主编马文斌教授,欢迎业界专家供稿与支持;转载需注明出处并保障文章的完整性。




还没有评论,来说两句吧...